Hoy: 23 de noviembre de 2024
Investigadores creen que un fármaco puede prevenir la sordera provocada por ruidos fuertes y el envejecimiento
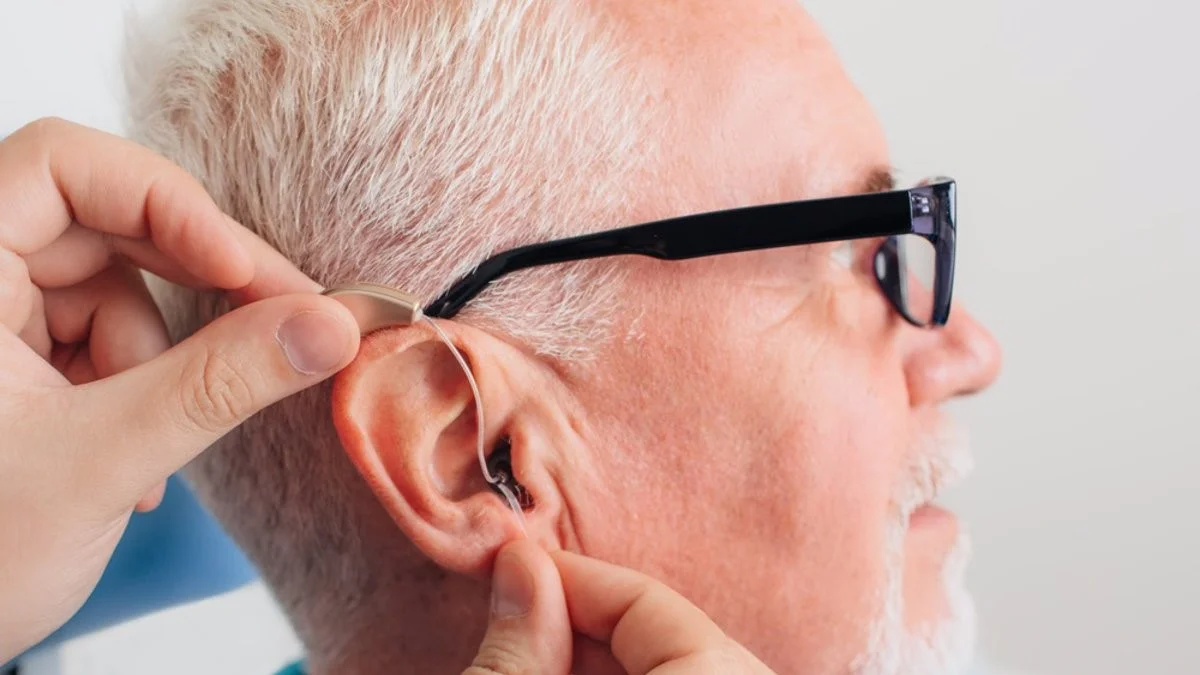
Descubren un gen, el TMTC4, que relaciona la falta de audición con la muerte celular en el oído interno, un hallazgo clave para analizar maneras de evitarla
Unos investigadores de la Universidad de California-San Francisco (UCSF) sugieren la posibilidad de que en un futuro un fármaco pueda prevenir la sordera provocada por ruidos fuertes y el envejecimiento. Han descubierto un gen, el TMTC4, que relaciona la falta de audición con la muerte celular en el oído interno. Un hallazgo que ayuda a analizar las maneras de evitarla.
La revista Journal of Clinical Investigation Insight ha publicado el trabajo de los investigadores, que relaciona estudios en animales sobre la pérdida de audición con un tipo raro de sordera hereditaria en humanos.
En ambos casos, las mutaciones en el gen TMTC4 desencadenan un efecto dominó molecular, conocido como respuesta a proteínas desdobladas (UPR, por sus siglas en inglés), que conduce a la muerte de las células ciliadas del oído interno.
Han comprobado que la pérdida de audición por exposición a ruidos fuertes o fármacos como el cisplatino, una forma común de quimioterapia, también se debe a la activación de la UPR en las células ciliadas. Algo que sugiere que la UPR puede estar detrás de varias formas diferentes de sordera.
Existen varios fármacos que bloquean la UPR y detienen la pérdida de audición en animales de laboratorio. Según los investigadores, los nuevos hallazgos refuerzan la necesidad de probar estos fármacos en humanos con riesgo a perder la audición.
Pruebas sólidas para prevenir la sordera
“Millones de adultos estadounidenses pierden audición cada año debido a la exposición al ruido o al envejecimiento, pero hasta ahora era un misterio qué estaba fallando”, afirma el doctor Dylan Chan, coautor principal del artículo y director del Centro de Comunicación Infantil (CCC) del Departamento de Otorrinolaringología de la UCSF. “Ahora tenemos pruebas sólidas de que TMTC4 es un gen de la sordera humana y de que la UPR es una auténtica diana para prevenirla”, señala.
En 2014, el director del Programa de Investigación del Desarrollo Cerebral de la UCSF y coautor principal del artículo, Elliott Sherr, observó que varios de sus pacientes jóvenes con malformaciones cerebrales tenían todos mutaciones en TMTC4. Aunque los estudios de laboratorio de este gen planteaban un interrogante.
“Esperábamos que los ratones con mutaciones en TMTC4 tuvieran graves defectos cerebrales desde el principio, como esos pacientes pediátricos. Sin embargo, para nuestra sorpresa, al principio parecían normales”, explica Sherr. “Pero a medida que esos animales crecían, vimos que no se sobresaltaban en respuesta a ruidos fuertes. Se habían quedado sordos después de madurar”, detalla.
Las causas de la pérdida acelerada de audición
Para indagar en su investigación, Sherr se asoció con Chan, experta en oído interno. El caso de estos animales parecía una versión acelerada de la pérdida de audición relacionada con la edad en humanos. Tras trabajar juntos, descubrieron las claves de este problema.
Demostraron que las mutaciones en TMTC4 y que el ruido fuerte inducían la autodestrucción de las células ciliadas del oído. En ambos casos, las células pilosas se inundaban con un exceso de calcio que desequilibraba otras señales celulares, como la UPR.
Ante este fenómeno, descubrieron una forma de impedir que los ratones se quedaran sordos con el ISRIB. Este fármaco, desarrollado en la UCSF, bloquea el mecanismo de autodestrucción de la UPR en lesiones cerebrales traumáticas.
El gen de la sordera que afecta a ratones y a humanos
En 2020, científicos surcoreanos unieron los hallazgos de Chan y Sherr de 2018 con mutaciones genéticas que encontraron en dos hermanos jóvenes con pérdida de audición. Las mutaciones estaban en TMTC4 y coincidían con lo que Chan y Sherr habían visto en animales. Aunque se diferenciaban de las de los pacientes de neurología pediátrica de Sherr.
“Es raro conectar tan rápidamente los estudios en ratones con los humanos”, afirma Sherr. “Gracias a nuestros colaboradores coreanos, pudimos demostrar más fácilmente la relevancia de nuestro trabajo para las muchas personas que se quedan sordas con el tiempo”, indica.
Contaron con la aportación de un otorrinolaringólogo de la Facultad de Medicina de la Universidad Nacional de Chungnam, en Corea. Este médico les facilitó el envío de células de esos pacientes a la UCSF. Sherr y Chan analizaron la actividad UPR de esas células. De esta forma, descubrieron que este tipo de mutación de TMTC4 activaba la UPR en humanos.
Cuando Chan y Sherr mutaron TMTC4 solo en las células ciliadas de ratones, estos se quedaron sordos. Al hacer lo mismo en células de miembros de la familia coreana que no eran sordos y en líneas celulares humanas de laboratorio, comprobaron que la UPR propició la autodestrucción de las células.
Por eso, concluyeron que el TMTC4 era un gen de la sordera tanto en ratones como en humanos. Y comprender sus mutaciones les proporciona una nueva forma de estudiar la sordera progresiva, fundamental para cuidar el oído interno adulto. Las mutaciones imitan los daños provocados por el ruido, por el envejecimiento o por fármacos como el cisplatino.
Esperanza en un medicamento eficaz en el futuro
Los investigadores imaginan un futuro en el que las personas que deban tomar cisplatino, o que se expongan a ruidos fuertes, tomen un medicamento que amortigüe la UPR. Para evitar de esta forma que sus células ciliadas se debiliten y, por tanto, para preservar su audición.
De momento, los científicos sugieren que la UPR se puede usar en otros contextos en los que las células nerviosas se saturan y mueren. Incluidas enfermedades que durante mucho tiempo se consideraron incurables, como el Alzheimer o la enfermedad de Lou Gehrig.